Електронний посібник для підготовки до ЗНО з біології (молекулярний і клітинний рівні)

РІВНІ ОРГАНІЗАЦІЇ ЖИВОЇ МАТЕРІЇ
Для будь-якої живої природи характерна складна ієрархічна супідрядність рівнів організації її структур.
Молекулярний рівень. Будь-яка жива система складається з біологічних макромолекул — нуклеїнових кислот, білків, полісахаридів та інших органічних речовин. З цього рівня починаються різноманітні процеси життєдіяльності організмів: обмін речовин, перетворення енергії, передача спадкової інформації.
Клітинний рівень. Клітина є структурно-функціональною одиницею всіх живих організмів, існуючих на Землі (виняток становлять віруси). На клітинному рівні сполучаються процеси передачі інформації та перетворення речовин і енергії.
Організмений рівень. Елементарною одиницею організмового рівня є особина (індивід), яка розглядається в розвитку — від моменту зародження до припинення існування — як жива система. На цьому рівні вивчають особину та властиві їй як цілому риси будови та поведінки.
Популяційно-видовий рівень. Популяція —надорганізмена система, в якій здійснюються елементарні еволюційні перетворення. На цьому рівні вивчають чинники, що впливають на чисельність популяцій, проблему збереження зникаючих видів, чинники мікроеволюції.
Біогеоценотичний рівень. На цьому рівні здійснюється взаємодія організмів між собою і з чинниками неживої природи, що визначають їх чисельність, видовий склад і продуктивність.
Біосферний рівень. Біосфера — сукупність усіх біогеоценозів, система, що охоплює всі явища життя на нашій планеті. На цьому рівні відбувається колообіг речовин і перетворення енергії, пов’язані з життєдіяльністю всіх живих організмів. (Виконати вправу)
ОСНОВНІ ВЛАСТИВОСТІ ЖИВИХ ОРГАНІЗМІВ
Єдність хімічного складу. До складу живих організмів входять ті ж хімічні елементи, що й до об’єктів неживої природи. Проте співвідношення елементів у живому та неживому неоднакове. Живі організми на 98 % складаються з Карбону, гідрогену, Оксигену і Нітрогену.
Обмін речовин і енергії. Важлива ознака живих систем — використання зовнішніх джерел речовини й енергії у вигляді їжі, світла тощо. Через живі системи проходять потоки речовин і енергії, отже, вони є відкритими. Основу обміну речовин складають взаємопов’язані й збалансовані процеси асиміляції (анаболізму) — синтезу з ви тратою енергії, і дисиміляції (катаболізму) — розпаду з виділенням енергії. Обмін речовин забезпечує відносну сталість хімічного складу організмів.
Самовідтворення. Існування кожної окремо взятої біологічної системи обмежене в часі. Підтримка життя пов’язана із самовідтворенням, завдяки якому життя виду не припиняється. В основі відтворення лежить спадковість — властивість перенесення інформації про ознаки організму від батьківської особини до дочірньої. Ця інформація закодована в структурі ДНК.
Мінливість. Відносна пристосованість організмів до середовища забезпечується мінливістю — здатністю набувати нових ознак і властивостей. Мінливість створює матеріал для природного добору.
Ріст і розвиток. Під ростом розуміється збільшення розмірів і маси особин із збереженням загальних рис будови. Ріст супроводжується розвитком, у результаті якого виникає новий якісний стан об’єкту. Розвиток живої форми матерії представлений індивідуальним та історичним розвитком. Протягом першого поступово і послідовно виявляються всі властивості організмів. Історичний розвиток супроводжується утворенням нового виду та прогресивним ускладненням життя.
Подразливість. Ця властивість виявляється активними реакціями живих організмів на зовнішню дію. Завдяки подразливості організми вибірково реагують на умови навколишнього середовища.
Дискретність. Будь-яка біологічна система складається з окремих взаємозв’язаних і взаємодіючих частин, які утворюють структурно-функціональну єдність.
Біологія клітини
Клітина — елементарна одиниця живого.
З відомих живих організмів тільки віруси є позаклітинними формами життя. Усі інші біологічні об’єкти побудовані з клітин — однієї (бактерії, найпростіші) або значної кількості (багатоклітинні тварини, рослини, гриби). Клітини різних організмів відрізняються за розмірами (від 0,5 мкм до 5 мм і більше), формою (видовжена, округла, неправильна), функціями (у багатоклітинних — опорна, видільна, захисна, транспортна тощо), тривалістю життя (від кількох годин до багатьох десятків років). Незважаючи на це клітини мають спільні властивості: здатність до самовідтворення та передачі генетичної інформації, обміну речо-
вин, росту, розвитку, мінливості, подразливості.
Історія вивчення клітини почалася в 1665 р., коли англійський природодослідник Роберт гук, вивчаючи під мікроскопом тонкий зріз корка, виявив, що він складається з маленьких комірок; це були перші клітини, побачені людиною. А через 200 років, у 1839 р., німецький фізіолог і цитолог Теодор Шванн сформулював основні положення клітинної теорії: — клітина — мікроскопічна жива система, що є структурно-функціональною одиницею ор-
ганізму;
— нові клітини утворюються в результаті поділу або злиття раніше існуючих;
— для всіх клітин характерна єдність хіміч- ного складу та метаболічних процесів;
— організм може складатися з однієї або безлічі клітин;
— багатоклітинні організми є системою клітин, які утворюють тканини й органи, пов’язані між собою гуморальними і нервовими типами регуляції;
— еволюція живих систем ішла шляхом ускладнення та диференціювання, від доядерних організмів до ядерних одноклітинних і далі до ядерних багатоклітинних.
ХІМІЧНИЙ СКЛАД КЛІТИНИ
Хімічні елементи
У живих клітинах виявлено понад 70 елементів періодичної системи Д. І. Менделєєва. За кількісним розподілом їх можна поділити на три групи.
Макроелементи (вміст понад 0,01 %): Карбон, гідроген, Оксиген, Нітроген, Фосфор, Сульфур, Натрій, Кальцій, Калій, Магній, Хлор.
Мікроелементи (10–2—10–6 %): Ферум, Цинк, Манган, Кобальт, Купрум, Флуор, йод. Ультрамікроелементи (менше за 10–6 %): Бор, Літій, Алюміній, Силіцій, Станум, Кадмій, Арсен, Селен, Ванадій, Титан, Хром, Нікель, Рубідій тощо.
Клітина — елементарна одиниця живого.
З відомих живих організмів тільки віруси є позаклітинними формами життя. Усі інші біологічні об’єкти побудовані з клітин — однієї (бактерії, найпростіші) або значної кількості (багатоклітинні тварини, рослини, гриби). Клітини різних ор-
ганізмів відрізняються за розмірами (від 0,5 мкм до 5 мм і більше), формою (видовжена, округла, неправильна), функціями (у багатоклітинних — опорна, видільна, захисна, транспортна тощо), тривалістю життя (від кількох годин до багатьох десятків років). Незважаючи на це клітини мають спільні властивості: здатність до самовідтворення та передачі генетичної інформації, обміну речовин, росту, розвитку, мінливості, подразливості.
Історія вивчення клітини почалася в 1665 р., коли англійський природодослідник Роберт гук, вивчаючи під мікроскопом тонкий зріз корка, виявив, що він складається з маленьких комірок; це були перші клітини, побачені людиною. А через 200 років, у 1839 р., німецький фізіолог і цитолог Теодор Шванн сформулював основні поло - ження клітинної теорії:
— клітина — мікроскопічна жива система, що є структурно-функціональною одиницею організму;
— нові клітини утворюються в результаті поділу або злиття раніше існуючих;
— для всіх клітин характерна єдність хімічного складу та метаболічних процесів;
— організм може складатися з однієї або безлічі клітин;
— багатоклітинні організми є системою клітин, які утворюють тканини й органи, пов’язані між собою гуморальними і нервовими типами регуляції;
— еволюція живих систем ішла шляхом ускладнення та диференціювання, від доядерних організмів до ядерних одноклітинних і далі до ядерних багатоклітинних.
Макроелементи є компонентами органічних сполук, беруть участь в утворенні зв’язків між білковими молекулами, біоелектричних процесах. Мікроелементи забезпечують перебіг ферментативних реакцій, входять до складу гормонів і вітамінів, беруть участь у процесах дихання. Біологічне значення багатьох ультрамікроелементів не встановлене.
Неорганічні речовини
До неорганічних речовин, що входять до складу живих клітин, належать вода та мінеральні
сполуки — солі Натрію, Калію, Кальцію, Магнію тощо.
Вода
Вода є основною неорганічною речовиною клітини, її вміст коливається від 40 % (механічна
тканина рослин, жирова тканина тварин) до 99 % (клітини медузи). Унікальні фізико-хімічні властивості води забезпечують її здатність виконувати різні функції.
Функції води
Метаболічна. Вода є середовищем для біохімічних реакцій (гідроліз, гідратація) і кінцевим продуктом багатьох біохімічних реакцій, а також донором електронів під час фотосинтезу. Речовини, розчинні у воді, називаються гідрофільними, нерозчинні у воді — гідрофобними.
Транспортна. Вода забезпечує перенесення біологічних молекул усередині клітин, з клітин, до клітин, крізь клітини, є головним компонентом транспортної системи вищих рослин і кровоносної системи тварин. Це можливо завдяки тому, що вода — універсальний розчинник і має високий коефіцієнт поверхневого натягу.
Механічна. Вода забезпечує пружний стан клітин і тканин рослин (тургор), є амортизатором під час механічних впливів на організм, послаблює тертя між дотичними поверхнями.
Терморегуляторна. Вода забезпечує рівномірний розподіл тепла, що виділяється під час екзотермічних процесів усередині організму, а під час випаровування з поверхні тіла тварин (потовиділення) або рослин (транспірація) охоло джує організм.
Мінеральні солі
Розчинні солі Калію, Натрію, Кальцію забезпечують найважливішу властивість живих клітин — подразливість. Слабколужна реакція внутрі шньоклітинного середовища зумовлюється
фосфат- і гідрогенофосфатіонами,міжклітинноїрідини та крові — карбонат- і гідрогенокарбонатіонами.
Нерозчинні мінеральні солі входять до складу міжклітинної речовини кісткової тканини, чере-
пашок молюсків, найпростіших, скелета губок.
Органічні речовини
Близько 90 % сухої маси клітин припадає на чотири типи органічних молекул: білки, ліпіди, вуглеводи, нуклеїнові кислоти. Крім того, у менших кількостях у клітинах містяться інші органічні сполуки, що відіграють важливу роль
у біохімічних процесах. До них належать органічні кислоти (піровиноградна, молочна, яблучна, лимонна, жирні кислоти — пальмітинова, стеаринова), пігменти (хлорофіл, білірубін) тощо. (Виконати вправу)
БІЛКИ (Переглянути відео)
Білки — це біологічні полімери, мономерами яких є амінокислоти.
Функції білків
Структурна. Білки утворюють основу цитоплазми і входять до складу клітинних органел і мембран. Сухожилля, суглобові зв’язки, кістки скелета, копита складаються з білків. Наприклад, білки колаген і еластин забезпечують пружність і пластичність шкіри, судин, зв’язок.
Каталітична. Біологічні каталізатори, що прискорюють біохімічні реакції, називаються ферментами. Усі ферменти є білками. Кожний фермент каталізує одну або декілька однотипних реакцій, тому зв’язування фермента із субстратом
(речовиною, що піддається ферментативному перетворенню) високоспецифічне. Ділянка молекули білка, яка відповідає за зв’язування із субстратом, називається активним центром, а комплекс, що утворився при цьому,— фермент-субстратним комплексом. У процесі реакції фермент не під- дається ані якісним, ані кількісним змінам.
Ферменти мають дуже високу активність, вони здатні послідовно каталізувати тисячі й навіть мільйони реакцій за секунду. При цьому вони функціонують у дуже вузькому інтервалі умов середовища й у разі їхньої зміни інактивуються.
Рухова. Будь-які форми активного руху в живій природі (робота м’язів, биття війок і джгутиків, рух хромосом під час клітинного поділу, внутрішньоклітинне переміщення цитоплазми) здійснюються скоротливими білковими структурами. Наприклад, основу поперечно-смугастої мускулатури складають білки актин і міозин, які переміщаються один щодо одного, що приводить до зміни лінійних розмірів м’яза.
Транспортна. Білок еритроцитів гемоглобін транспортує кисень від легенів до тканин і органів, сироватковий білок альбумін здійснює транспорт жирних кислот. Білки клітинних мембран виконують вибіркове перенесення речовин
(глюкози, амінокислот, йонів) через ліпідний бішар.
Захисна. Захист організму від дії інфекції та підтримка гомеостазу забезпечуються реакціями імунітету. Найважливішими чинниками гуморального імунітету є антитіла — білки, які маркірують чужорідні біополімери — антигени. Захисну функцію також виконують білки, що безпосередньо руйнують клітини (лізоцим слини) або блокують процеси біосинтезу (інтерферон в інфікованих вірусами клітинах).
Регуляторна. Багато з гормонів є білками (інсулін, глюкагон, соматотропін). Вони регулюють перебіг фізіологічних процесів — ріст клітин, інтенсивність обміну речовин.
Запасаюча. Білки здатні накопичуватися як запасний матеріал для живлення організму, що розвивається (яєчний альбумін, білки насіння рослин).
Енергетична. Білки розщеплюються для добування енергії у виняткових випадках, якщо в організмі в результаті тривалого голодування вичерпані запаси вуглеводів і жирів. Енергетична цінність 1 г білка складає близько 17 кДж.
Рецепторна. Багато білків на поверхні плазматичної мембрани клітин здатні пізнавати молекули певної структури. Специфічними рецепторами розпізнаються молекули гормонів і медіаторів (як правило, один рецептор може пізнавати тільки один тип молекул — рецептор адреналіну розпізнає тільки адреналін, рецептор інсуліну — тільки інсулін). Білкові рецептори на поверхні
клітин імунної системи здатні пізнавати чужорідний антиген і запускати реакцію його знищення.
Структура білків
У звичайній еукаріотичній клітині налічується близько 10 тис. різних білків, а загальна кількість відомих білкових молекул наближається до 50 тис.
Усі ці білки складаються не більше ніж з двадцяти видів амінокислот. Амінокислоти є органічними молекулами, що мають загальну схему будови.
Вони містять карбоксильну групу —COOHй аміногрупу —NH2, зв’язані з атомом Карбону.
Індивідуальні властивості кожної амінокислоти визначаються радикалом R. Залежно від структури радикала всі амінокислоти поділяють на полярні та неполярні. Послідовно сполучаючись між собою, амінокислоти формують молекулу білка. При цьому зв’язок утворюється між аміногрупою однієї амінокислоти та карбоксильною групою іншої з виділенням молекули води. Зв’язок —CO—NH— називається пептидним.
Рівні структурної організації білків
Розрізняють декілька рівнів структурної організації білків.
Первинна с т р у к т у р а. Утворений у процесі трансляції поліпептидний ланцюг — послідовність амінокислот, з’єднаних між собою пептидними зв’язками, називають первинною структурою білка. Первинна структура будь-якого білка закодована в молекулі ДНК. Білкові молекули містять від 100 до 1500 амінокислот. Якщо в поліпептидному ланцюзі менше за 70 амінокислот, таку молекулу називають пептидом.
Вторинна структура. Розрізняють два види вторинної структури білка — α-спіраль і β-складчастий шар (β-структура).
Білкова α-спіраль стабілізується водневими зв’язками, які утворюються між атомом гідрогену групи —NH однієї амінокислоти й атомом Оксигену групи —C=O іншої. Радикали амінокислот не беруть участі у формуванні водневих зв’язків і обернені назовні від спіралі. Такий тип вторинної структури мають міозин і тропоміозин — м’язові білки, які беруть участь у процесах скорочення, кератин — структурний білок волосся, нігтів, дзьоба, пір’я і рогів.
Поліпептидний ланцюг (ланцюги) у β-структурі має зигзагоподібну конфігурацію (структуру складчастого листка). Він також стабілізується водневими зв’язками. Ділянки поліпептидного ланцюга, які прилягають одна до одної, у β-структурі можуть бути як паралельними (йдуть в одному напрямі), так і антипаралельними (йдуть у протилежних напрямах). Прикладом білка, який має тільки β-складчасту вторинну структуру, є фіброїн — білок шовку, що виділяється шовковичними залозами гусениць шовкопряда під час формування коконів.
Третинною структурою білка називається тривимірна упаковка поліпептидного ланцюга, тобто укладання в просторі α-спіральних і β-структурних ділянок молекули. Третинна структура стабілізується й утримується чотирма типами зв’язків, які утворюються між радикалами амінокислот:
1) дисульфідні зв’язки між атомами Сульфуру двох залишків цистеїну;
2) водневі зв’язки, що утворюються за участю атома гідрогену амінокислотних радикалів;
3) гідрофобні взаємодії між радикалами неполярних амінокислот;
4) електростатичні (йонні) взаємодії між різнойменно зарядженими групами радикалів полярних амінокислот (аспарагінової, глутамінової кислот, аргініну, лізину, гистидіну).
За просторовою формою третинної структури білки поділяються на глобулярні, поліпептидні ланцюги яких згорнуті в компактні сферичні або еліпсоподібні структури (інсулін, альбумін, усі ферменти), і фібрилярні, поліпептидні ланцюги яких, розташовуючись уздовж однієї осі, утворюють довгі волокна (фібрили) або шари (колаген, еластин, міозин, фібрин).
Четвертинна структура. Деякі білки складаються не з одного, а з декількох поліпептидних ланцюгів, що кодуються різними генами (гемоглобін, велика кількість ферментів вуглеводного обміну). У цьому випадку говорять про четвертинну структуру білка, а поліпептидні ланцюги, що його утворюють, називають субодиницями. Четвертинна структура утворюється тільки після закінчення формування третинних структур окремих субодиниць і стабілізуєтьсягідрофобними й електростатичними взаємодіями.
Денатурація
На стабільність білкової молекули впливає безліч чинників. Так, під впливом температури, механічного тиску, хімічних агентів відбувається порушення просторової організації молекули — четвертинної, третинної, вторинної структур із збереженням первинної; білок втрачає свої фізико-хімічні та біологічні властивості. Це явище називається денатурацією. Якщо денатуруючий агент припиняє свою дію, в деяких випадках білок набуває початкової просторової конфігурації та відновлює біологічну активність. Процес відновлення фізико-хімічних і біологічнихвластивостейбілканазиваєтьсяренатурацією. Якщо дія чинників приводить до порушення первинної структури білка, то говорять про протеоліз. Протеоліз білків відбувається, наприклад, під впливом ферментів шлунка або лізосом.
ВУГЛЕВОДИ (Виконайте вправу)
До вуглеводів належать альдегіди та кетони багатоатомних спиртів, а також полімери цих сполук із загальною формулою Cn(H2O)m. Вміст вуглеводів у тваринних клітинах рідко перевищує 5 %, але в рослинних може досягати 90 % від загальної кількості органічних молекул.
Функції вуглеводів
Енергетична. Під час окиснення у процесі клітинного дихання вуглеводи вивільняють енергію, яка в них міститься, забезпечуючи значну частину енергетичних потреб організму.
Захисна. В’язкі секрети (слизи), багаті на вуглеводи, оберігають стінки органів (шлунок, кишечник, бронхи) від механічних і хімічних впливів.
Рецепторна. Більшість клітинних рецепторів є глікопротеїнами. Зв’язуючись з інтегральними мембранними білками, вуглеводи у складі рецепторів беруть участь у розпізнаванні сигнальних молекул (гормонів, нейромедіаторів).
С т р у к т у р н а . Вуглеводи є основними структурними компонентами клітин, які утворюють опорні тканини (целюлоза, хітин). Запасаюча. Відкладаючись у тканинах, вуглеводи можуть забезпечити організм енергією у разі голодування (крохмаль, глікоген).
Класифікація вуглеводів
Вуглеводи поділяють на моносахариди, олігосахариди та полісахариди. Моносахариди — це прості вуглеводи. У молекулі моносахариду може бути від трьох до дев’яти атомів Карбону, але найбільш поширені п’яти- та шестикарбонові моносахариди. Залежно від кількості атомів Карбону, які утворюють скелет молекули, моносахариди поділяють на тріози, тетрози, пентози, гексози і т. д. Моносахариди важливі як джерело енергії, а також як будівельні блоки для синтезу полісахаридів. Велике значення мають пентози рибоза і дезоксирибоза, що входять до складу ДНК і РНК. Із гексоз найпоширеніші глюкоза, фруктоза та галактоза, які є просторовими ізомерами та мають молекулярну формулу C6 H12O6 . глюкоза (виноградний цукор) зустрічається у тварин і рослин; вона є основним джерелом енергії для клітин. Фруктоза у великій кількості міститься в плодах покритонасінних рослин; у клітинах багатьох тварин і рослин вона може ферментативно перетворюватися на глюкозу.
Олігосахариди — це вуглеводи, які мають від двох до десяти ланок моносахаридів. Зв’язок між двома моносахаридами здійснюється через атом Оксигену та називається глікозидним. Олігосахариди, що складаються з двох моносахаридів, називаються дисахаридами. До дисахаридів належать: 1) лактоза (молочний цукор), що міститься в молоці, утворена залишками глюкози та галактози; 2) значно поширена в рослинному світі сахароза (тростинний цукор C12H22O11), що складається з глюкози та фруктози; 3) продукт часткового гідролізу крохмалю в рослинах — мальтоза.
Полісахариди — високомолекулярні сполуки, які містять понад десять моносахаридних ланок. Вони складають основну масу вуглеводів, що зустрічаються в живих клітинах. Полісахариди головним чином виконують функцію резерву їжі й енергії (крохмаль, глікоген), а також використовуються як будівельний матеріал (целюлоза, хітин).
Крохмаль, полімер глюкози, має формулу (C6H10O5)n. Він є резервною поживною речовиною рослин і міститься в клітинах у вигляді різних за формою та розмірами крохмальних зерен. Крохмаль знаходить широке застосування в медицині та в багатьох галузях промисловості (харчовій, паперовій, фармацевтичній тощо). У промислових масштабах його отримують із бульб картоплі та зерен кукурудзи.
Глікоген є полімером глюкози, але з більш розгалуженим, ніж у крохмалю, ланцюгом мономерів. Це головний енергетичний і вуглеводний резерв людини та тварин. Особливо великий вміст глікогену в печінці (до 10 %) і м’язах (до 4 %). Зустрічається він у грибів і мікроорганізмів.
Целюлоза — структурний полісахарид клітинної стінки рослин, полімер глюкози. На її частку припадає близько 50 % усього органічного вуглецю біосфери. Целюлоза має величезне значення для господарської діяльності людини, складаючи основну масу бавовняних тканин, паперу, штучного шовку, деяких пластмас і вибухових речовин.
НУКЛЕЇНОВІ КИСЛОТИ (Виконати вправу)
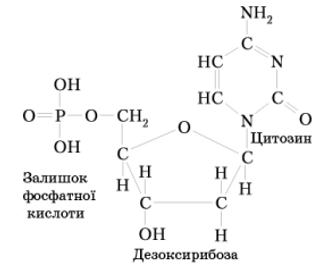
Н у к л е ї н о в і к и с л о т и — це біополімери, мономерами яких є нуклеотиди. Кожний нуклеотид складається з п’ятивуглецевого моносахариду, азотистої основи та залишку фосфатної кислоти.
Залежно від виду моносахариду нуклеїнові кислоти поділяють на дві групи:
1) рибонуклеїнові кислоти (РНК), що містять рибозу;
2) дезоксирибонуклеїнові кислоти (ДНК), до складу яких входить дезоксирибоза. Азотисті основи є похідними пурину та піримідину. До пуринових основ належать аденін (А) і гуанін (г), до піримідинових — цитозин (Ц), урацил (У), тимін (Т). До складу ДНК входять аденін, гуанін, цитозин, тимін; у РНК замість тиміну міститься урацил. Нітратні основи приєднуються до 1′ -карбонового атома, а фосфатна кислота — до 5′ -карбонового атома рибози або дезоксирибози.
Нуклеотиди об’єднуються в полімерні ланцюги шляхом утворення фосфодіефірних зв’язків між фосфатною групою одного нуклеотиду і 3′ -гідроксигрупою цукру іншого нуклеотиду. Через таку будову полінуклеотидний ланцюг має певний напрям. На одному його кінці залишається вільна фосфатна кислота, приєднана до 5′ -OH-групи цукру (початок ланцюга), на іншому — 3′ -ОН-група (кінець ланцюга).
Дезоксирибонуклеїнова кислота (ДнК) (Переглянути відео)
У 1953 р. американський біохімік Джеймс Уотсон і англійський фізик Френсіс Крік запропонували модель організації ДНК, відповідно до якої:
1) кожна молекула ДНК складається з двох антипаралельних полінуклеотидних ланцюгів, які утворюють подвійну спіраль;
2) кожний нуклеотид розташований у площині, перпендикулярній до осі спіралі; 3) два полінуклеотидні ланцюги сполучені водневими зв’язками, які утворюються між нітратними основами різних ланцюгів;
4) взаємодія азотистих основ специфічна: пуринова основа може сполучатися тільки з піримідиновою, і навпаки. Такий принцип сполучання основ називається принципом комплементарності;
5) послідовність основ одного полінуклеотидного ланцюга може значно варіювати, але послідовність їх у другому ланцюзі чітко комплементарна першій. Два полінуклеотидні ланцюги в молекулі ДНК сполучаються між собою за допомогою водневих зв’язків між відповідними азотистими основами: аденін взаємодіє з тиміном за допомогою двох водневих зв’язків, цитозин з гуаніном — за допомогою трьох. При цьому утворюється по двійна спіраль, полінуклеотидні ланцюги в якій орієнтовані антипаралельно.
Рибонуклеїнова кислота (РнК)
РНК міститься у всіх живих клітинах у вигляді одноланцюгових молекул. Залежно від структури та функції РНК поділяють на матричну, або інформаційну (мРНК, або іРНК), рибосомну (рРНК) і транспортну (тРНК). Інформаційна РНК синтезується в ядрі клітини на матриці одного з ланцюгів ДНК, тобто є комплементарною певному її фрагменту. Далі вона транспортується в цитоплазму і сама служить матрицею для синтезу білка. Рибосомна РНК входить до складу рибосом, беручи участь у трансляції. Транспортна РНК відповідає за доставку певної амінокислоти до рибосоми та включення її в утворений поліпептидний ланцюг. У структурі тРНК є комплементарні послідовності нуклеотидів, які взаємодіють з утворенням специфічної просторової структури тРНК (наявність декількох «шпильок»), що нагадує листок конюшини. На одній із шпильок розташований нуклеотидний триплет — антикодон, на протилежному кінці — послідовність для специфічного зв’язування амінокислоти.
Аденозинтрифосфорна кислота (атФ)
АТФ за структурою є нуклеотидом. Молекула АТФ складається з моносахариду рибози, нітратної основи аденіну і трьох послідовно зв’язаних залишків фосфатної кислоти.
Основна функція АТФ полягає в акумуляції енергії, що виділяється під час різних біохімічних реакцій (розщеплення вуглеводів і жирів, фотосинтезу). Численні процеси, які відбуваються в клітині (проведення нервового імпульсу, м’язове скорочення, транспорт речовин, синтез білка), вимагають надходження енергії, яка міститься в хімічних зв’язках молекули АТФ. Зв’язки, під час розриву яких виділяється велика кількість енергії, називаються макроергічними. АТФ виконує свою функцію шляхом ферментативного відщеплення кінцевої фосфатної групи; при цьому утворюється аденозиндифосфорна кислота (АДФ), а енергія, що вивільняється, використовується для здійснення біохімічних реакцій. Відокремлена фосфатна група може потім знову приєднатися до АДФ з утворенням АТФ. При цьому використовується енергія, яка виділяється в результаті розщеплення, наприклад, вуглеводів і ліпідів.
ЛІПІДИ
Ліпіди — органічні сполуки, різні за структурою, хімічною будовою, функціями, але схожі за фізико-хімічними властивостями: нерозчинні у воді, добре розчинні в органічних розчинниках (ефірі, хлороформі, ацетоні).
Функції ліпідів
Енергетична. У разі повного окиснення 1 г тріацилгліцеролу виділяється 38,9 кДж 92 енергії, що приблизно вдвічі більше, ніж під час окиснення 1 г білків або вуглеводів.
Структурна. Ліпіди є основними структурними компонентами біологічних мембран.
Регуляторна. Ліпіди регулюють текучість мембран, є важливими внутрішньоклітинними сигнальними молекулами, компонентами мієлінових оболонок нервових клітин, попередниками гормонів, вітамінами, беруть участь у регуляції генної активності.
Запасаюча. Завдяки високій енергетичній цінності жири є енергетичним депо й ендогенним джерелом води (у разі окиснення 100 г жиру виділяється 107 г води). Захисна. Жири є основним компонентом підшкірної клітковини, вони запобігають тепловтратам і захищають від механічних впливів.
Класифікація ліпідів
За хімічною будовою ліпіди поділяють на прості та складні. Д о простих ліпідів належать: 1) тріацилгліцероли (тригліцериди, або жири) — ефіри гліцерину та жирних кислот; 2) воски — ефіри жирних кислот і довголанцюгових спиртів; 3) вітаміни А, Е, К.
Тріацилгліцероли (жири) зустрічаються як у тварин, так і в рослин. Жири тваринного походження тверді (вершкове масло, свиняче сало), оскільки до їхнього складу входять переважно насичені жирні кислоти, що мають високу температуру плавлення. До складу рослинних жирів входять переважно ненасичені жирні кислоти, які мають нижчу температуру плавлення. Тому ці жири рідкі (соняшникова, оливкова, бавовняна й інші рослинні олії). Неполярні молекули тріацилгліцеролів виконують запасаючу та терморегуляторну функції.
Д о складних ліпідів належать: 1) стероїди (холестерол, статеві гормони, вітамін D); 2) фосфоліпіди, до складу яких окрім гліцеролу та жирних кислот входять залишок фосфатної кислоти й нітрогеновмісні сполуки (фосфатідилсерин, фосфатідилетаноламін, фосфатідилхолін тощо); 3) гліколіпіди — комплекси ліпідів з вуглеводами.
БУДОВА КЛІТИНИ
Клітини всіх живих організмів за структурно-функціональними особливостями можна поділити на дві великі групи: еукаріотичні та прокаріотичні. Структурними компонентами еукаріотичних клітин є плазматична мембрана, цитоплазма, клітинні органели, ядро. Прокаріотичні клітини не мають ядра та деяких органел (мітохондрій, ендоплазматичного ретикулуму, апарату гольджі). У цьому розділі розглядається біологія еукаріотичних клітин.
ПЛАЗМАТИЧНА МЕМБРАНА (Переглянути відео)
Плазматична мембрана (плазмалема) оточує клітину, визначає її розміри, форму та виконує такі функції:
бар’єрну (захисну) — забезпечує асиметричний розподіл речовин між внутрішньоклітинним і позаклітинним середовищами;
транспортну — визначає вибіркове надходження молекул до клітини та з клітини;
рецепторну — уловлює і підсилює сигнали, закодовані в хімічній структурі гормонів, медіаторів;
комунікативну — здійснює контакт сусідніх клітин між собою і з позаклітинною речовиною. Забезпечення вказаних функцій безпосередньо пов’язане з будовою плазматичної мембрани.
Будова плазматичної мембрани.
Усі біологічні мембрани становлять собою ансамблі ліпідних і білкових молекул, які з’єднуються разом за допомогою нековалентних взаємодій.
Молекули фосфоліпідів утворюють безперервний подвійний шар завтовшки 4—5 нм. Полярні головки фосфоліпідів у ліпідному бішарі орієнтовані назовні та контактують з молекулами води, а неполярні (гідрофобні) хвости жирних кислот спрямовані один до одного. Ліпідний бішар є ефективним бар’єром для всіх водорозчинних 93 молекул. гідрофобні речовини (стероїдні гормони, жирні кислоти) легко проникають крізь площину бішару. У ліпідний матрикс включені також молекули холестеролу, які виконують стабілізуючу функцію шляхом зменшення текучості мембран.
У ліпідний бішар занурені численні білкові молекули. Білки, які наскрізь пронизують бішар, називаються інтегральними (трансмембранними), а мембрани, що розташовані на зовнішній або внутрішній поверхні, — периферичними. Білки відповідають за пізнавання сигнальних молекул (рецепторну функцію часто виконують глікопротеїни), за зв’язок плазмалеми із цито скелетом і з міжклітинною речовиною, за ви бірковий транспорт речовин.
Транспорт речовин
Різні молекули можуть транспортуватися крізь плазматичну мембрану пасивно, тобто шляхом дифузії, або активно — з використанням енергії АТФ.
Пасивний транспорт. Рушійною силою дифузійного перенесення речовин є різниця їх концентрацій по обидва боки мембрани. гідрофобні речовини і, напевне, вода проникають у клітину або виводяться з неї безпосередньо крізь ліпідний бішар, а гідрофільні проходять через специфічні канали — утворені інтегральними білками пори, які пронизують мембрану наскрізь. Такі канали забезпечують контакт внутрішньоклітинного вмісту із зовнішнім середовищем. Активний транспорт. Це пов’язане із споживанням енергії перенесення молекул або йонів крізь мембрану проти градієнта концентрації. Енергія необхідна для подолання намагання речовини дифундувати в протилежному напрямі. Прикладом системи активного транспорту може бути натрій-калієвий насос, виявлений у клітинах живих організмів. У клітинах підтримується висока концентрація йонів Калію, а в позаклітинному середовищі переважаючим йоном є Натрій. Тому Калій по градієнту концентрації намагається залишити клітину, а Натрій — проникнути в неї. Натрій-калієвий насос — інтегральний білок, який викачує з клітини Натрій в обмін на надходження Калію. Він приводиться в дію енергією АТФ. Більш як третина АТФ, яку споживає тваринна клітина в стані спокою, ви трачається на роботу натрій-калієвого насоса. Підтримка концентрацій цих іонів на певному рівні необхідна для збереження клітинного об’єму, електричної активності в нервових і м’язових клітинах, активного транспорту деяких речовин (моносахаридів, амінокислот).
Особливими видами активного транспорту є ендоцитоз і екзоцитоз, за допомогою яких різні речовини переносяться крізь мембрану в клітини (ендоцитоз) або з них (екзоцитоз). У разі ендоцитозу плазматична мембрана вгинається всередину, утворює поглиблення (інвагінації), які потім, відокремлюючись, перетворюються на вакуолі — наповнені рідиною мембранні пухирці. Розрізняють два види ендоцитозу — фагоцитоз (захоплення твердих частинок) і піноцитоз (поглинання рідких речовин). Останній є найбільш характерним для амебоїдних клітин і для клітин, які беруть участь у водно-сольовому обміні (клітини печінки, нирок).
Екзоцитоз — процес, зворотний ендоцитозу, його функція — виведення з клітин різних речовин. Шляхом екзоцитозу з травних вакуолей у найпростіших виділяються неперетравлені залишки, з клітин травних залоз — травні секрети та ферменти, з клітин ендокринної системи — гормони.
ЦИТОПЛАЗМА ТА КЛІТИННІ ОРГАНЕЛИ
Цитоплазма — простір клітини, розміщений між плазматичною мембраною та ядром.
У цитоплазму занурені клітинні органели та різні непостійні структури — включення. Частину цитоплазми, яка міститься між органелами і є складною колоїдною системою, часто називають цитозолем. У цитозолі містяться вуглеводи, ліпіди, РНК, АТФ, органічні кислоти, численні білкові молекули. Деякі білки утворюють тривимірну сітку — цитоскелет, зв’язаний із плазмалемою, ядром і органелами.
Функції цитоплазми
Комунікативна — забезпечує зв’язок різних частин клітини (компартментів) між собою.
Гомеостатична — підтримує сталість хіміч ного складу та фізичних властивостей усередині клітини.
Транспортна — забезпечує перенесення біомолекул між органелами.
Органели (органоїди) — постійні клітинні структури, що забезпечують виконання специфічних функцій у процесі життєдіяльності клітини. Органели еукаріотичної клітини можна поділити на мембранні та немембранні. Перші, у свою чергу, можуть бути одномембранними, оточеними однією мембраною (лізосоми, апарат гольджі, ендоплазматичний ретикулум), і двомембранними, відокремленими від цитозолю зовнішньою 94 і внутрішньою мембранами (мітохондрії, хлоропласти). До структури немембранних органоїдів мембрани не входять (рибосоми, клітинний центр, органели руху).
Клітинні включення — компоненти цитоплазми, які становлять собою відкладення речовин, тимчасово виведених з метаболізму, або кінцевих продуктів метаболізму. Найпоширеніші включення — ліпідні краплі, що складаються з нерозчинних у воді молекул жирів, і гранули глікогену, кожна з яких є єдиною дуже розгалуженою молекулою. У рослинних клітинах часто зустрічаються крохмальні зерна та кристали кальцій оксалату.
ЕНДОПЛАЗМАТИЧНИЙ РЕТИКУЛУМ (ЕПР)
Ендоплазматичний ретикулум (ендоплазматична сітка) — система дрібних вакуолей і канальців, сполучених один з одним і відмежованих від цитозолю однією мембраною.
Мембрана ЕПР має численні складки, вигини й утворює одну безперервну поверхню, яка оточує єдину замкнену порожнину — порожнину ЕПР. Мембрана ЕПР переходить у зовнішню ядерну мембрану, складаючи з нею одне ціле. Розрізняють шорсткий (гранулярний) і гладенький (агранулярний) ЕПР. Шорсткий ЕПР вкритий рибосомами, розташованими на повернутому до цитоплазми боці мембрани. його основна функція — участь у синтезі білка. Окрім цього, шорсткий ЕПР необхідний для транспорту макромолекул у різні ділянки клітини (лізосоми, апарат гольджі), синтезу структурних компонентів клітинних мембран. Шорсткий ЕПР розвинений у спеціалізованих клітинах, які секретують білки (клітини підшлункової залози, клітини, що продукують антитіла) або інтенсивно утворюють мембрани (палички сітківки ока).
Гладенький ЕПР можна розглядати як вільну від рибосом ділянку шорсткого ЕПР. Він бере участь у завершальних етапах синтезу ліпідів і деяких внутрішньоклітинних полісахаридів. гладенький ЕПР переважає над шорстким у гепатоцитах, клітинах кіркової речовини надниркових залоз. Він добре розвинений у поперечносмугастих м’язових волокнах, оскільки здатний поглинати йони кальцію із цитозолю, що приводить до розслаблення міофібрил під час кожного м’язового скорочення.
Апарат Гольджі (АГ)
Апарат (комплекс) Гольджі — це група мембранних мішечків — цистерн, зв’язаних із системою пухирців (пухирців Гольджі), локалізованих біля клітинного ядра.
Основна функція Аг — транспорт речовин і хімічні перетворення клітинних полімерів. Особливо розвинений Аг в секреторних клітинах, наприклад в гепатоцитах. Із ЕПР в Аг транспортуються речовини, призначені для секреції. Тут вони модифікуються і виводяться з пухирцями гольджі шляхом екзоцитозу. Іноді Аг бере участь у транспорті ліпідів.
Крім транспортної, апарат гольджі виконує такі функції: 1) синтез глікопротеїнів; 2) депонування речовин і їх перерозподіл між різними ділянками клітини; 3) формування лізосом, у яких неактивні травні ферменти перетворюються на активні.
Лізосоми
Лізосоми — округлі одномембранні пухирці, наповнені травними ферментами, які здійснюють розщеплення білків, вуглеводів, нуклеїнових кислот, ліпідів на амінокислоти, моносахариди, нуклеотиди, гліцерин і жирні кислоти. Лізосомальні ферменти синтезуються на шорсткомуЕПР і транспортуються його каналами до Аг. Пізніше від Аг відгалужуються пухирці, які перетворюються на лізосоми. Такі первинні лізосоми зливаються з вакуолями, що утворилися в процесі ендоцитозу. При цьому формується вторинна лізосома. Лізосомальні ферменти перетравлюють вміст вакуолі, а неперетравлені залишки виводяться шляхом екзоцитозу. У деяких організмів неутилізовані відходи можуть не виводитися з клітини, а збиратися в залишкових тільцях — особливому виді клітинних включень.
Лізосоми є ефективним засобом знищення антигенів — хвороботворних мікроорганізмів, які фагоцитуються макрофагами.
Рибосоми
Рибосоми — органели, що забезпечують синтез білка.
Рибосоми складаються з двох субодиниць: великої та малої. Кожна субодиниця становить собою складний комплекс із багатьох білків і молекул рибосомної РНК (рРНК). Збирання субодиниць з утворенням функціонально-активної рибосоми відбувається під час взаємодії з молекулою іРНК. У цитоплазмі клітини рибосоми можуть розташовуватися вільно або бути прикріпленими до зовнішньої поверхні мембрани шорсткого ЕПР. Окрім цитоплазми, рибосоми містяться також у хлоропластах і мітохондріях.
Мітохондрії
Мітохондрії — органели, основна функція яких полягає в забезпеченні клітин енергією. Мітохондрія складається із зовнішньої та внутрішньої мембран, між якими є міжмембранний простір, і внутрішнього вмісту — мітохондріального матриксу.
Зовнішня мембрана мітохондрій гладка. Вона має високу проникність для багатьох молекул, що містяться в цитозолі (зокрема для невеликих білків), тому за хімічним складом міжмембранний простір практично не відрізняється від цитоплазматичного. Внутрішня мембрана мітохондрій утворює численні складки, або заглиблення — кристи, що значно збільшують площу її поверхні. Мембрана непроникна для білків, полісахаридів і багатьох іонів. У внутрішню мембрану вбудовані ферменти дихального ланцюга, що забезпечують синтез АТФ. Тут також містяться білки, які відповідають за транспорт до матрикса молекул піровиноградної кислоти, іонів Ca2+, Mg2+.
Матрикс є колоїдною системою, в якій містяться: 1) кільцеві молекули ДНК (мітохондріальний геном) і ферментні системи, що забезпечують їхню реплікацію та транскрипцію; 2) різні види РНК (тРНК, іРНК); рибосоми, відмінні від рибосом цитоплазми; 3) метаболічні ферменти.
ДНК мітохондрій замкнута в кільце і представлена в кожній мітохондрії кількома копіями. Вона містить близько 40 генів (у ссавців), достатніх для кодування лише невеликої частини мітохондріальних білків. Більшість білків, що забезпечують функцію мітохондрій, кодуються ядерною ДНК і доправляються в матрикс із цитоплазми.
У мітохондріальному матриксі містяться ферменти, що забезпечують перебіг численних біохімічних процесів: реакцій циклу трикарбонових кислот, утворення ацетил-КоА з пірувату, розщеплення і синтезу жирних кислот.
Мітохондрії добре розвинені в клітинах, діяльність яких пов’язана зі споживанням великої кількості енергії. Так, у міоцитах вони утворюють тривимірні сітки, розташовані по периферії міофібрил.
Клітинний центр (центросома)
Клітинний центр визначає орієнтацію веретена поділу і розходження хромосом до полюсів клітини під час мітозу або мейозу. Крім того, він бере участь у формуванні органоїдів руху — джгутиків і війок.
Зазвичай клітинний центр знаходиться поблизу ядра тваринних клітин. Він складається з двох розташованих під прямим кутом одна до одної центріолей. Кожна центріоль — це циліндр завдовжки 0,3 мкм і діаметром 0,1 мкм, стінка якого утворена дев’ятьма групами білкових мікротрубочок. Центріолі оточені аморфним простором (хмарою) з білків, вуглеводів і невеликої кількості ліпідів, що відіграє важливу роль у прикріпленні ниточок веретена поділу. Важливою особливістю центріолей є їхня здатність до автономного розмноження, яке не залежить від поділу клітини.
Органели руху
Псевдоподії (несправжні ніжки) утворюються шляхом вигину плазматичної мембрани. Серед вільноживучих одноклітинних організмів псевдоподії має амеба. Вони є також у лейкоцитів ссавців.
Джгутики (у рослин і тварин) і війки (у тварин) мають схожу будову — декілька (частіше 11) мікротрубочок, здатних скорочуватись, які відрізняються одна від одної тільки довжиною. Зовні мікротрубочки покриті мембраною — продовженням плазмалеми. головна функція цих органел полягає в пересуванні клітин або в просуванні вздовж клітин частинок і рідини, що їх оточує. Так, за допомогою джгутиків пересуваються сперматозоїди; миготливим епітелієм з війчастих клітин покриті дихальні шляхи. Основа джгутика або війки закріплюється в цитоплазмі за допомогою базального тільця, яке являє собою центріоль.
Ядро (Переглянути відео)
Ядро — частина еукаріотичних клітин, що несе спадкову інформацію, закладену в молекулі ДНК.
Деякі клітини еукаріотів (еритроцити ссавців, клітини ситоподібних трубок рослин) не містять ядра. Проте показано, що втрата ядра вторинна і спрямована на забезпечення виконання клітиною певних функцій.
Рідкий вміст ядра (ядерний сік, або нуклеоплазма) відокремлений від цитозолю ядерною оболонкою. Ядерна оболонка утворена 96 двома мембранами — зовнішньою і внутрішньою — і пронизана ядерними порами діаметром 60—100 нм. Зовнішня мембрана з одного боку переходить у мембрани ЕПР, а з іншого (по краях ядерних пор) — у внутрішню мембрану. Крізь ядерні пори відбувається обмін різними органічними молекулами (білки, іРНК) і надмолекулярними комплексами (субодиниці рибосом) між нуклеоплазмою і цитозолем.
У нуклеоплазмі містяться: 1) хроматин — молекули ДНК, зв’язані з білками-гісто нами;
2) одне або декілька ядерець — круглястих структур (їх не можна вважати окремими органелами),
у яких відбувається синтез рРНК, її упаковка і початкові етапи збирання рибосомних субодиниць;
3) ферментні системи, що забезпечують реплікацію, транскрипцію і репарацію ДНК. (3D модель ядра)







Особливості будови рослинної клітини
Рослинну клітину зовні покриває клітинна стінка, яка складається з полісахариду целюлози. Живий вміст клітини називається протопластом. До органел, типових для рослинної клітини, належать вакуолі та пластиди.
Наявність клітинної оболонки, вакуолей і плазмодесм — тонких цитоплазматичних містків, що сполучають сусідні клітини — зумовлена прикріпленим способом життя та відсутністю скелета у рослин. Також характерною особливістю рослинних клітин є ріст переважно шляхом розтягування за рахунок збільшення розміру вакуолей, а не за рахунок збільшення об’єму цитоплазми.
Вакуоля може займати до 90 % об’єму клітини, її основними функціями є: підтримка тургору — внутрішнього тиску клітини, і складування продуктів життєдіяльності клітини. Клітинний сік, що наповнює вакуолю, являє собою водний розчин, який має слабкокислу або нейтральну реакцію. Хімічний склад, в’язкість і концентрація розчинених у клітинному соку речовин відмінні від таких у цитоплазмі, що зумовлено вибірною проникністю вакуолярної мембрани. До речовин, які можуть міститися в клітинному соку, належать алкалоїди (кофеїн,
хінін, атропін, морфін) і пігменти антоціани, які надають клітинному соку синього та фіолетового забарвлення.
Пластиди (переглянути відео) є органелами, характерними тільки для рослин і деяких інших еукаріотів з автотрофним способом живлення. Найважливішими для життєдіяльності клітини пластидами є хлоропласти, що містять зелений фотосинтезуючий пігмент хлорофіл. Хлоропласти зустрічаються, як правило, у всіх освітлених частинах рослини. Хлоропласти належать до двомембранних органел, внутрішня речовина хлоропласту називається стромою. Внутрішня мембрана хлоропластів утворює впорядковану систему порожнин дископодібної форми, які називають тилакоїдами, що зібрані в стопки — грани.
Лейкопласти являють собою безбарвні пластиди, розташовані, як правило, у прихованих від сонячного світла частинах рослини. Внутрішня структура лейкопласту розвинена слабко, основною функцією є запасання поживних речовин — крохмалю, жирів, білків.
Хромопласти — пластиди, які містять різні барвникові пігменти, що належать до групи каротиноїдів. Розташовуються в забарвлених частинах рослини (плодах, пелюстках), позбавлені хлорофілу, внутрішня мембранна система не розвинена.
Характерною особливістю пластид є їхня здатність перетворюватися одна на одну. Вона зумовлена тим, що в результаті еволюції лейко- і хромопласти утворилися з хлоропластів. Найтиповішими видами перетворень є перетворення
лейкопластів на хлоропласти і хлоропластів на хромопласти.
ДНК: ОРГАНІЗАЦІЯ, РЕПЛІКАЦІЯ, ТРАНСКРИПЦІЯ, РЕПАРАЦІЯ
(3D модель рослинної клітини)
Організація ДНК
Сукупність ДНК у будь-якій клітині організму називають геномом, а терміном генотип позначають закладену в геномі генетичну інформацію.
У ядрах більшості еукаріотичних клітин ДНК перебувають у вигляді хромосом. Число хромосом у клітинах організмів дуже варіює. Повний набір хромосом у ядрі еукаріотичної клітини називають
каріотипом. В еукаріотичних організмах ДНК міститься в комплексі з ядерними білками — гістонами.
Гістони утворюють «котушки», на які намотується спіраль. Комплекс ядерної ДНК з гістонами називають хроматином. Нитки хроматину, у свою чергу, зібрані у впорядковані петлі. Певні ділянки хроматину прикріпляються до внутрішньої мембрани ядерної оболонки.
На певній стадії клітинного циклу (метафаза) нитки хроматину, що складають хромосоми, упаковуються так щільно, що стають видимими у світловий мікроскоп (метафазні хромосоми).
Генетичний код
У ДНК у зашифрованому вигляді записана інформація про всі білки, що синтезуються клітиною. Послідовність нуклеотидів ДНК ви значає амінокислотну послідовність білків. Залежність між основами нуклеотидів та амінокислотами
називається генетичним кодом.
Основні властивості генетичного коду:
1) Кожна амінокислота кодується послідовністю з трьох нуклеотидів, яка називається триплетом, або кодоном.
2) У всіх організмах одні й ті самі амінокислоти кодуються одними й тими ж кодонами, тобто код універсальний.
3) Код є виродженим — одна амінокислота кодується більш ніж одним триплетом
(виключення — метіонін і триптофан).
4) Код однозначний — кожний кодон (триплет) кодує тільки одну амінокислоту.
5) Код не перекривається: кодони зчитуються один за одним. Наприклад, за послідовністю АУггЦАЦгА зчитування відбувається тільки у такий спосіб: АУг/гЦА/ЦгА.
Зчитування АУг/Угг/ггЦ або АУг/ггЦ /ЦАЦ неможливе.
Структура гена
Ділянка ДНК, яка несе інформацію про амінокислотну послідовність будь-якого білка, називається ген.
ген еукаріотичних організмів має складну будову. Він складається з декількох частин:
промотора — ділянки ДНК, що несе певну сигнальну послідовність нуклеотидів, яка пізнається ферментом транскрипції РНК-полімеразою;
екзонів — власне кодуючих ділянок гена, що несуть смислові послідовності ДНК;
інтронів — ділянок ДНК, які не несуть інформації про структуру білка і згодом видаляються з молекули іРНК;
термінатора — ділянки, яка містить сигнальну послідовність про припинення транскрипції РНК-полімеразою (стоп-кодон).
Гени розташовуються лінійно, йдучи або відразу один за одним (у цьому випадку говорять про генні сегменти), або розділяючись послідовностями некодуючої ДНК.
Реплікація ДНК (переглянути відео)
Реплікація ДНК — процес, під час якого молекули ДНК подвоюються. Подвоєння ДНК, що відбувається на певній стадії клітинного циклу, необхідне для передачі спадкової інформації з покоління в покоління.
Реплікація здійснюється особливим ферментним комплексом — ДНК-полімеразою, і відбувається у декілька етапів. На першому етапі ДНК-полімераза прикріплюється до молекули ДНК у певних ділянках — точках початку реплікації. Кожна хромосома еукаріотів містить декілька таких ділянок, так що в процесі реплікації одночасно беруть участь багато полімераз. Далі на невеликій ділянці ланцюга ДНК розходяться — формується реплікаційна виделка. Полімераза, використовуючи кожний із ланцюгів як матрицю, починає синтезувати дочірні ланцюги, комплементарно добудовуючи дедалі нові нуклеотиди.
Реплікаційна виделка просувається вздовж ДНК доти, поки не зустрінеться з іншою реплікаційною виделкою або не дійде до кінця хромосоми. У результаті реплікації утворюються дві дочірні спіралі, кожна з яких містить один ланцюг матричної молекули й один заново синтезований ланцюг (тому реплікація ДНК називається напівконсервативною).
Репарація ДНК
Незважаючи на те що з ДНК зв’язана велика кількість гістонових білків, її структура все ж таки недостатньо стабільна. Причини різних дефектів в укладанні ДНК зумовлені: броунівським рухом атомів, які її складають; підвищенням температури в клітині; дією хімічних речовин (алкілсульфонатів, нітрозосечовини); дією ультрафіолетового проміння та іонізуючої радіації.
Усунення пошкоджень молекули ДНК називається репарацією. В основі процесів репарації лежить комплементарність нітратних основ. У разі порушення структури пурину або піримідину спеціалізовані ферменти (ендонуклеази, глікозилази) вирізають його та проводять заміну, використовуючи як матрицю протилежний ланцюг.
Транскрипція ДНК
Транскрипція — процес синтезу іРНК на матриці ДНК.
Утворені молекули іРНК у свою чергу є матрицями для синтезу білка. Транскрипцію здійснює фермент РНК-полімераза. Процес транскрипції відбувається у декілька етапів. Спочатку РНКполімераза розпізнає ген, який несе інформацію про потрібний клітині білок. Це можливо завдяки
сигнальній послідовності нуклеотидів промотора. Приєднавшись до промотора, РНК-полімераза розкручує певну ділянку подвійної спіралі ДНК і починає добудовувати до однієї з них комплементарні нуклеотиди. Почавши копіювання, РНК-полімераза продовжує добудовувати комплементарні нуклеотиди доти, доки не зустріне стоп-сигнал (термінатор). Після цього полімераза відходить від ДНК,
а утворений попередник молекули іРНК зазнає в ядрі подальших модифікацій.
гени, які кодують рРНК, представлені в геномі великою кількістю копій, зібраних у сегменти (кластери). Під час одноразового проходження РНК-полімерази транскрибується відразу безліч молекул рРНК, які потім розрізаються і зв’язуються з білками, що приводить до формування рибосомальних суб одиниць. Складання рибосомальних субодиниць відбувається, таким чином, у ядрі, а саме в тій його специфічній ділянці, яка називається ядерцем.
ВІДТВОРЕННЯ КЛІТИН
Клітина, як структурно-функціональна одиниця живого, здатна до самовідтворення, яке здійснюється шляхом поділу. В еукаріотичних клітин
існують два способи поділу — мітоз і ме йоз. Стосовно клітин, які діляться шляхом мітозу, вживається поняття клітинний цикл — період життя клітини від її утворення до моменту поділу.
Клітинний цикл
Клітинний цикл складається з інтерфази і власне мітотичного поділу (мітозу). Інтерфаза складається з трьох періодів: передсинтетичного G1, синтетичного S і постсинтетичного G2.
Передсинтетичний період характеризується інтенсивним ростом клітини, активним синтезом білків, збільшенням об’єму цитоплазми та площі клітинних мембран. Він є найтривалішим і складає основну частину життя переважної більшості клітин.
Далі йде синтетичний період, під час якого відбувається реплікація ДНК і формування Х-подібних хромосом. Кожна хромосома складається тепер з двох сестринських хроматид, ідентичних одна одній. У певній ділянці — центромері —
обидві хроматиди залишаються сполученими одна з одною. У цей період хромосоми ще тонкі, дуже зігнуті й їх не видно у світловий мікроскоп.
У постсинтетичному періоді інтерфази синтезуються білки веретена поділу й достатня кількість АТФ (процес поділу клітини надзвичайно
складний та енергоємний). Після закінчення інтерфази починається власне мітотичний поділ (мітоз).
Мітоз (переглянути відео)
Мітоз — спосіб клітинного поділу, під час якого клітини, що утворюються, ідентичні за генотипом і є точною копією материнської клітини. Мітоз відбувається у декілька стадій (фаз), які безперервно переходять одна в одну.
Профаза. У цей період центріолі клітинного центру розходяться до протилежних полюсів клітини. Оболонка ядра поступово розпадається на маленькі мембранні пухирці; аналогічні зміни відбуваються з апаратом гольджі й ендоплазматичним ретикулумом. У хромосомах спостерігається конденсація хроматину. Процеси транскрипції повністю припиняються, й утворення необхідних клітині білків може здійснюватися тільки за рахунок раніше синтезованих молекул іРНК.
Метафаза. У метафазі конденсація хроматину максимальна. Утворюються так звані метафазні хромосоми, які добре видно у світловий мікроскоп. Кожна хромосома складається з двох сестринських хроматид, які утворюють плечі хромосоми, центромери і кінцевих ділянок — теломерів. Положення центромери і довжина плечей різні у різних хромосом, це є надійним критерієм для їх
ідентифікації. Під час метафази хромосоми вибудовуються на екваторі клітини. Формується веретено поділу — білкові нитки (мікротрубочки), що тягнуться від центріолей до центромер хромосом. При цьо му до кожної центромери може прикріплятися декілька ниточок.
Анафаза. В анафазі подвійні хромосоми розриваються веретеном поділу і сестринські хроматиди відходять до протилежних полюсів клітини. При
цьому вони орієнтовані центромерами до відповідного полюса, а теломерами — до екватора клітини.
Телофаза. У телофазі навколо хромосом починає формуватися ядерна оболонка, з’являються ядерні пори, відновлюється парність центріолей, цитоплазма й органели рівномірно розподіляються між полюсами клітини. Хромосоми поступово деспіралізуються, починають формуватися ядерця. Далі йде процес розділу цитоплазми з утворенням двох дочірніх клітин — цитокінез. Утворені дочірні клітини вступають в інтерфазу.
Біологічне значення мітозу полягає в підтримуванні сталої кількості хромосом у клітинних поколіннях — дочірні клітини отримують таку ж генетичну інформацію, яка міститься в ядрі материнської клітини. У багатьох еукаріотичних організмів виявлений так званий прямий поділ, або амітоз, під час якого відбувається подвоєння ДНК, формування нових ядер, проте утворення дочірніх клітин не відбувається або генетичний матеріал розподіляється між ними нерівномірно. У результаті амітозу з’являються багатоядерні клітини, характер-
ні для деяких тканин тварин, грибів і рослин.
Мейоз (переглянути відео)
Мейоз — спосіб поділу клітин, під час якого відбувається зменшення (редукція) кількості хромосом і перехід клітин з диплоїдного стану
в гаплоїдний. Мейоз включає два поділи — редукційний (перший) і екваційний (другий). Кожний із них поділяється на ряд стадій (фаз): профазу, метафазу, анафазу і телофазу. Ці стадії першого поділу позначаються римською цифрою I, другого — цифрою II.
Процеси, що йдуть в інтерфазі I мейозу, ідентичні таким під час мітозу.
Профаза I. Спостерігається попарне зближення подвоєних гомологічних і спіралізованих хромосом (утворення бівалентів). Відбувається кросинговер — злиття й обмін гомологічними ділянками. Руйнується ядерна оболонка, розхо-
дяться центріолі.
Метафаза I. Біваленти гомологічних хромосом розташовуються на екваторі клітини, нитки веретена поділу прикріплюються до центромер.
Анафаза I. До полюсів клітини розходяться подвоєні хромосоми (не сестринські хроматиди, як у мітозі) — по одній хромосомі з кожного біваленту. Відбувається двократне зменшення (редукція) кількості хромосом і їх випадковий пере-
розподіл у майбутніх гаметах.
Телофаза I. Утворюються дочірні клітини вже з гаплоїдним набором хромосом. Кожна хромосома складається з двох сестринських хроматид, ідентичних одна одній.
Після першого редукційного поділу мейозу клітини вступають у коротку інтерфазу II, яка не супроводжується подвоєнням ДНК. Потім починається другий поділ — екваційний. В анафазі II дочірні хроматиди розходяться до протилежних
полюсів клітини, а в телофазі II з двох клітин, що виникли під час редукційного поділу, утворюються чотири клітини, які несуть гаплоїдний набір хромосом.
Мейоз здійснюється під час утворення статевих клітин у тварин і спор у багатьох рослин (нестатеве розмноження).
(Скласти пазли) (Виконати тест)
ОБМІН РЕЧОВИН У КЛІТИНІ
Обмін речовин (метаболізм) — сукупність хімічних перетворень, які відбуваються в клітинах та забезпечують їхній ріст, життєдіяльність і відтворення.
Обмін речовин живої клітини складається з двох протилежно направлених видів реакцій — катаболічних і анаболічних. Сукупність реакцій розпаду органічних сполук називається катаболізмом або енергетичним обміном. Сукупність реакцій синтезу органічних сполук називається анаболізмом або пластичним обміном. Під час розщеплення (катаболізму) органічних сполук (білків, жирів,
вуглеводів) виділяється енергія, яка акумулюється в хімічних зв’язках молекул АТФ. Ця енергія використовується клітиною в анаболічних процесах — синтезі власних, необхідних на даний момент часу білків, жирів і вуглеводів. Таким чином, енергетичний і пластичний обмін тісно пов’язані між собою потоками речовини й енергії. За способом добування енергії живі організми
поділяються на автотрофів і гетеротрофів. Клітини гетеротрофів (тварини, гриби, більшість бактерій, паразитичні рослини) для побудови власних біополімерів використовують мономери поглинених і розщеплених ними органічних сполук, а також енергію, що виділяється при цьому. Автотрофи здатні синтезувати власні біополімери з води, вуглекислого газу та мінеральних солей. Залежно від джерела енергії, яка використовується, автотрофи поділяють на фототрофів (акумулюють сонячну енергію — зелені рослини, деякі бактерії) і хемотрофів (акумулюють енергію, що виділяється внаслідок окисно-відновних процесів,— сіркобактерії, нітрифікуючі бактерії).
За чутливістю до концентрації кисню в навколишньому середовищі всі організми поділяються на аеробів і анаеробів. Аероби можуть існувати тільки за наявності достатнього вмісту кисню.
Анаероби поділяються на облігатних (існують тільки в безкисневих умовах) і факультативних (здатні до життя в широкому діапазоні концент-
рацій кисню).
Обмін вуглеводів
Енергетичний обмін вуглеводів
Виділяють три етапи катаболізму вуглеводів.
На першому етапі полісахариди розщеплюються до моносахаридів. У більшості багатоклітинних гетеротрофних організмів ці процеси відбуваються в травному тракті й називаються порожнинним травленням, в одноклітинних автотрофів і гетеротрофів — безпосередньо всередині клітини.
На другому етапі глюкоза під дією ряду цитоплазматичних ферментів перетворюється на піровиноградну кислоту (піруват). Процес розщеплення глюкози до пірувату називають анаеробним гліколізом, оскільки для його здійснення не по трібний кисень. У безкисневих умовах
піруват, що утворився, перетворюється на молочну кислоту (лактат), яка виводиться з клітин як кінцевий продукт катаболізму вуглеводів. Під час розщеплення 1 молекули глюкози шляхом анаеробного гліколізу утворюється 2 молекули піровино градної кислоти, виділяється 2 молекули АТФ і 2 молекули нікотинамідаденіндинуклеотиду — НАДН. Пізніше НАДН може бути використаний клітиною для синтезу АТФ. Деякі прокаріоти (анаеробні грампозитивні бактерії роду Clostrydium) й еукаріоти (дріжджі) окиснюють глюкозу з утворенням етилового спирту. Такий процес називається спиртовим бродінням. При цьому глюкоза перетворюється на піруват, а потім ферментативно окиснюється спочатку до оцтового альдегіду, а потім до етилового спирту. Із 1 молекули глюкози утворюється 2 молекули АТФ, вуглекислий газ і вода. Спиртове бродіння широко застосовується для добування спирту, пива та вина.
Третій етап катаболізму починається за наявності в середовищі достатньої кількості кисню. Утворений піруват надходить у мітохондрії та бере участь у реакції утворення ацетилкоферменту А (ацетил-КоА) — сульфуровмісної моле-
кули з макроергічним зв’язком, похідної оцтової кислоти. Ацетил-КоА піддається комплексу ферментативних перетворень, які об’єднуються під
назвою цикл Кребса або цикл трикарбонових кислот (ЦТК), у процесі яких утворюються 1 молекула АТФ, 3 молекули НАДН, 1 молекула флавінаденіндинуклеотиду — ФАДН2 і вуглекислий газ. НАДН і ФАДН2 пізнаються і зв’язуються ферментами дихального ланцюга мітохондрій, де окиснюються до НАД+ і ФАД+.
Дихальний ланцюг мітохондрій складається з декількох білкових комплексів, розташованих у внутрішній мембрані мітохондрій і здатних уловлювати і транспортувати електрони. Останній здійснює передачу електронів безпосередньо
на молекулярний кисень (О2) з утворенням води. Такий процес називають окисним фосфорилуванням. У разі окиснення 1 молекули НАДН утворюються 3 молекули АТФ, а у разі окиснення ФАДН2 — 2 молекули АТФ.
Пластичний обмін вуглеводів у гетеротрофних організмів
Моносахариди, які потрапили в цитоплазму, можуть не тільки піддаватися розщепленню з виділенням енергії, але й є матеріалом для синтезу власних полісахаридів клітини. Глюкоза за допомогою специфічних ферментів
полімеризується з утворенням глікогену (цей процес називається глікогенезом). У цьому разі витрачається енергія АТФ. Синтезований глікоген накопичується в цитозолі у вигляді гранул і є запасною поживною речовиною. У разі необхідності
він окиснюється до глюкози, яка включається в гліколіз. Утворена внаслідок розпаду глікогену в клітинах печінки ссавців глюкоза виходить у кров і є джерелом енергії для нейронів і м’язів. Оскільки більшість реакцій гліколізу є оборотними, клітина здатна синтезувати глюкозу з інших сполук ацетил-КоА, кислот, залучених у ЦТК (цей процес називається глюконео генезом).
Пластичний обмін вуглеводів у фототрофних організмів — фотосинтез
Фотосинтез (переглянути відео) — це процес перетворення енергії сонячного світла на енергію хімічних зв’язків і синтезу органічних сполук (вуглеводів) з неор- ганічних (вода та вуглекислий газ). Основним фотосинтетичним пігментом вищих рослин є хлорофіл. За хімічною структурою розрізняють декілька видів хлорофілу — а (міститься в хлоропластах усіх зелених рослин і ціанобактерій), b, с і d (присутні разом із хлорофілом а у клітинах водоростей).
Процес фотосинтезу складається з двох взаємопов’язаних етапів світлової та темнової фаз. Світлова фаза відбувається лише за наявності світла, за допомогою фотосинтетичних пігментів у тилакоїдах хлоропластів. Реакції темнової фази не
вимагають для свого здійснення світла та відбуваються в стромі хлоропластів. Сумарні рівняння світлової та темнової фаз:
У світловій фазі фотосинтезу відбувається поглинання світла молекулами хлорофілу і трансформація енергії світла в хімічну енергію ATФ і відновленого НАДФН (нікотинамідаденіндинуклеотидфосфат відновлений). Ці процеси здійснюються білковими комплексами, які входять до складу тилакоїдів хлоропластів.
Одними з таких комплексів є фотосистема 1 (ФС1) і фотосистема 2 (ФС2). У кожній фотосистемі виділяють три зони: антенний комплекс, реакційний центр, первинні акцептори електронів. Антенний комплекс складається з хлорофілу b і допоміжних пігментів. Він призначений для уловлювання енергії світла та передачі її на реакційний центр. До реакційного центру ФС1 і ФС2 входять молекули хлорофілу а. Процеси у світловій фазі здійснюються за так званою Z-схемою. Кванти світла, потрапляючи на ФС2 і передаючи їй свою енергію, збуджують електрони реакційного центру, які передаються через ланцюг білкових переносників і втрачають при цьому енергію. Утворене внаслідок виходу електронів вакантне місце у ФС2 поповнюється електронами, отриманими під час фотолізу води — реакції розщеплення молекули води під дією кванта світла з виділенням протонів, електронів і кисню. Рівняння фотолізу води має такий вигляд:
Водночас у разі збудження реакційного центру ФС1 електрон передається через ферумвмісні білки, також втрачаючи при цьому енергію. Частина енергії, що виділилася, йде на ферментативне відновлення НАДФ+ до НАДФН. Вакантне
місце, що утворилося у ФС1, займається електронами, що надійшли з ФС2. Енергія, що вивільнилася під час проходження електронів з ФС2 у ФС1, використовується для синтезу ATФ з AДФ і неорганічного фосфату. Утворені в результаті фотохімічних реакцій ATФ і НАДФН використовуються для здійснення реакцій темнової фази, в якій відбувається відновлення молекул СО2 до молекул вуглеводів (глюкози). Існують різні способи відновлення СО2, найпоширеніший із них — цикл Кальвіна, притаманний усім рослинам.
У процесі цикла Кальвіна відбувається фіксація атома Карбону CO2 для побудови глюкози (C6H12O6) з рибульозо-1,5-дифосфату (C5H8O5P2).
Для синтезу 1 молекули глюкози в циклі Кальвіна необхідно 12 молекул НАДФН і 18 молекул АТФ, що утворюються в результаті фотохімічних реакцій фотосинтезу. Енергія для синтезу вуглеводів утворюється внаслідок розщеплення молекул
АТФ, синтезованих під час проходження електронів по компонентах ФС1 і ФС2.
Утворена в процесі циклу Кальвіна глюкоза може потім розщеплюватися допирувата, надходити в цикл Кребса.
ОБМІН ЖИРІВ
Енергетичний обмін жирів (переглянути відео)
Жирні кислоти в клітинах гетеротрофів транспортуються в мітохондрії за допомогою специфічного переносника, де піддаються окисненню з утворенням ацетил-КоА, який надходить у цикл Кребса (у разі окиснення 1 молекули пальмітинової кислоти до СО2 і води утворюється 140 молекул АТФ). Цикл Кребса, таким чином, є універсальним клітинним циклом, який сполучає між
собою обмін вуглеводів і жирів. Процес розщеплення жирних кислот може відбуватися тільки в аеробних умовах.
Пластичний обмін жирів
Ацетил-КоА може правити за джерело для синтезу жирних кислот і холестеролу (а також стероїдних гормонів у відповідних клітинах ендокринних залоз). У жировій тканині жирні кислоти та глюкоза перетворюються на тріацилгліцероли
і запасаються у формі ліпідних (жирових) крапель доти, доки не будуть затребувані іншими органами. У разі голодування тріацилгліцероли жирової
тканини хребетних і деяких безхребетних тварин розщеплюються до жирних кислот і гліцеролу, які виходять у кров і слугують джерелом енергії для міокарду (у клітинах печінки гліцерол також здатний перетворюватися на глюкозу). Тріацилгліцероли можуть частково синтезуватися з глюкози у разі її окиснення до ацетил-КоА.
ОБМІН БІЛКІВ
Пластичний обмін (переглянути відео) — синтез білка Амінокислоти, що утворюються внаслідок розщеплення харчового білка гетеротрофами, транспортуються в цитоплазму клітин. Далі вони включаються в синтез клітинних білків. Замінні амінокислоти можуть утворюватися в клітині з різних речовин. Незамінні амінокислоти обов’язково мають надходити в гетеротрофні клітини з навколишнього середовища. Для різних організмів незамінними є різні амінокислоти. Клітини автотрофів здатні самостійно синтезувати всі необхідні амінокислоти, використовуючи нітратні сполуки, поглинені з ґрунту. При цьому витрачається енергія, акумульована в хімічних зв’язках АТФ у процесі фотосинтезу. Процес синтезу білка складається з декількох етапів:
1) транскрипція іРНК на матриці ДНК;
2) транспорт іРНК через ядерні пори в цитоплазму клітини;
3) формування комплексу іРНК з великою і малою субодиницями рибосом;
4) трансляція — процес реалізації інформації, закодованої в нуклеотидній послідовності іРНК, в амінокислотну послідовність білка;
5) посттрансляційні модифікації синтезованої білкової молекули.
Транскрипція іРнК та її модифікації
РНК-полімераза копіює не лише нуклеотиди екзонів, але також й інтронів. Тому молекула, що утворюється при цьому, містить не тільки кодуючі, але й «безглузді» послідовності. Особливі ферменти ядра здатні пізнавати інтрони та вирізати їх.
В ядрі іРНК піддається й іншим модифікаціям: до її кінців прикріплюються сигнальні послідовності нуклеотидів, які відповідають за подальші сполучання іРНК з рибосомою та її транспорт з ядра.
Транспорт іРнК
Зрілі молекули іРНК пізнаються особливими білками ядерних пор, які сприяють їх просуванню в цитоплазму за допомогою активного транспорту. Потрапивши в цитоплазму, іРНК зв’язується з рибосомальними субодиницями, це є сигналом
для збирання цих субодиниць у функціонально активну рибосому.
Трансляція
У процесі трансляції нуклеотидна послідовність іРНК зчитується групами по три нуклеотиди, у міру того як рибосома переміщається вздовж
молекули іРНК. Транспорт амінокислот до рибосом забезпечують тРНК. Для кожної амінокислоти існує специфічна тРНК. Молекули тРНК містять близько 80 нуклеотидів. Усі молекули мають подібну структуру: у кожної є акцепторна ділянка, до якої приєднується відповідна амінокислота, ділянка, що містить антикодон — послідовність з трьох нуклеотидів, комплементарну кодону іРНК, який відповідає певній амінокислоті.
Транспортна РНК з приєднаною до неї амінокислотою надходить до рибосоми та зв’язується антикодоном із комплементарним триплетом (кодоном) молекули іРНК. Зв’язування відбувається в чітко визначеному місці — на так званій А-ділянці рибосоми. У цей момент на Р-ділянці (вона розташована поряд з А-ділян-
кою) вже є тРНК, яка утримує кінець поліпептидного ланцюга, який росте. Амінокислота, закріплена на тРНК, яка щойно надійшла, утворює пептидний зв’язок з СООН-кінцевою амінокислотою поліпептидного ланцюга, і тРНК, яка
до цього була розташована на Р-ділянці, відділяється від рибосоми і здатна транспортувати іншу таку ж амінокислоту. Це приводить до переміщення тРНК, що залишилася (з якою тепер зв’язані амінокислоти синтезованого білка), на
Р-ділянку, що звільнилася. Тепер А-ділянка доступна для прикріплення наступної молекули тРНК, антикодон якої комплементарний кодону іРНК (остання також перемістилася відносно А-ділянки на один триплет). Так триває доти, доки в А-ділянці рибосоми не опиниться кодон іРНК, який не кодує жодної амінокислоти — стоп-кодон. В еукаріотів стоп-кодонами є триплети УАА, УАг і УгА. Для них не існує комплементарного антикодону тРНК; відсутність тРНК в А-ділянці викликає відщеплення поліпептидного ланцюга від тРНК, що знаходиться в Р-ді-
лянці. Трансляція припиняється.
Для більшості клітин синтез білка — найбільш енергоємний з усіх біосинтетичних процесів. Утворення кожного нового пептидного зв’язку супроводжується розщепленням щонайменше 4 молекул АТФ: 2 з них витрачаються на приєднання амінокислоти до відповідної тРНК, а ще 2 — на зв’язок тРНК з А-ділянкою і пересування рибосоми вздовж ланцюга іРНК.
Збирання одного білка триває в середньому від 20 до 560 секунд. Але навіть ця величезна швидкість може бути збільшена, якщо синтез поліпептидного ланцюга відбувається на полірибосомальному комплексі (полісомі). В останньому випадку нова рибосома приєднується до молекули іРНК відразу ж після того, як попередня зв’яже між собою достатню кількість амінокислот, щоб звільнити їй місце (це відповідає приблизно 80 нуклеотидам).
Посттрансляційні модифікації.
Після закінчення трансляції до утвореної молекули білка можуть приєднуватися різні органічні молекули — вуглеводи, жирні кислоти тощо. Цей процес відбувається в ендоплазматичному ретикулумі й апараті гольджі та називається посттрансляційною модифікацією.








